公司新闻 首页 > 新闻动态 > 公司新闻
韩国夫妇打造千亿市值药企,与默沙东签下大单,开启狂飙模式
今年4月,福布斯发布2024韩国富豪榜,韩国生物制药公司Alteogen的联合创始人兼首席执行官Park Soon-jae(朴顺载)博士首次进入榜单,是四位新上榜者中唯一一位来自制药行业的。
这还要得益于Alteogen公司在2024年2月官宣了与美国制药巨头默沙东达成一项利润丰厚的新合作。根据新的合作条款,默沙东将获得Alteogen专有的重组人透明质酸酶ALT-B4的全球独家许可,以开发和商业化“K药”(Keytruda,帕博利珠单抗)的皮下注射制剂。Alteogen将获得2000万美元的首付款,并有资格获得高达4.32亿美元的额外里程碑付款,以及基于产品销售的特许权使用费。(双方此前的合作为非独家许可)Alteogen首席执行官Park博士曾向媒体表示,这项合作有望实现韩国生物技术史上最大规模的技术费收入。
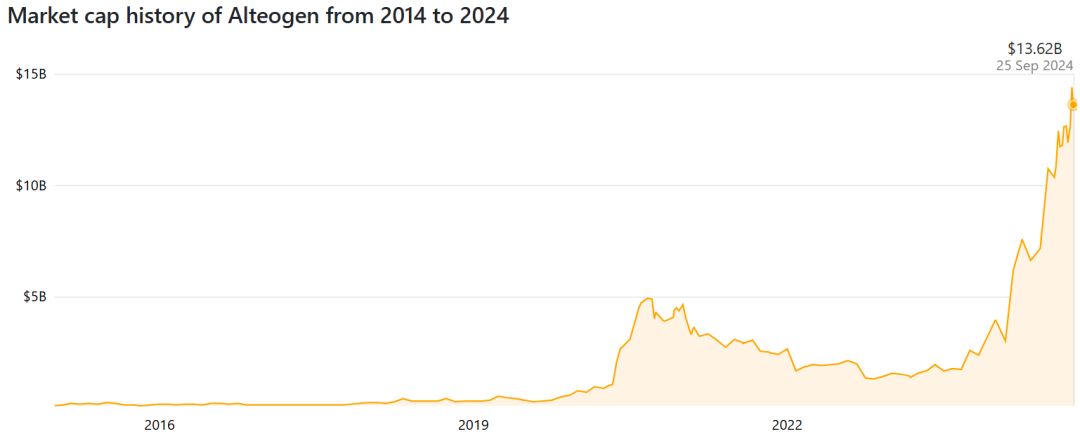
合作官宣之后,Alteogen公司股价飙升,创始人Park博士家族净资产随之增长,Park博士跻身亿万富翁行列。截至2024年9月25日,该公司市值达到136.2亿美元(近千亿人民币市值)。
回想到2024年初,韩国食品巨头Orion Group(好丽友集团)宣布斥资约4.18亿美元(约合30亿人民币)收购LegoChem Biosciences公司25.7%的股份,成为LegoChem的第一大股东。其实在此之前,好丽友曾与Alteogen有过股权投资谈判,不过最终谈判陷入了僵局。
Alteogen由Park Soon-jae博士与他的妻子ChungHye-Shin(郑惠信)博士在2008年5月共同创立,二人均拥有普渡大学生物化学博士学位。Chung博士曾担任公司首席科学官,她开发了该公司的长效蛋白质药物技术NexP™。据报道,Chung博士已在2023年9月离开了Alteogen,并在2024年3月将所持的3%的股份以3164亿韩元(约合2.3424亿美元)出售给了境外机构投资者。
首席执行官Park博士在生物医学研发方面拥有超过25年的经验,他最初在LG化学和LG生命科学担任高级研究员,并成功开发了人生长激素、促红细胞生成素和肝炎疫苗等重组生物药。在LG生命科学就职的后期,Park博士负责管理海外业务发展和合作以及许可,与各种制药和生物技术公司建立业务网络,并积累了业务发展经验。离开LG生命科学之后,他还协助韩华集团开展抗体生物类似药业务,建立了相关组织和管线。他被公认为是韩国生物医学研发和商业化的领军人物之一,被选为2010年由韩国国家工程院颁发的“韩国60年最具影响力100项技术和人物”之一。

2014年12月,Alteogen在科斯达克上市(KOSDAQ:196170)。目前该公司已是一家技术领先的生物制药公司,专注于行业前沿领域,主要开发三类产品:改良的长效生物制剂(称为Bio-better)、ADC药物和抗体生物类似药,并与国内外生物制药相关企业进行联合研究、开发、CMO委托生产等。
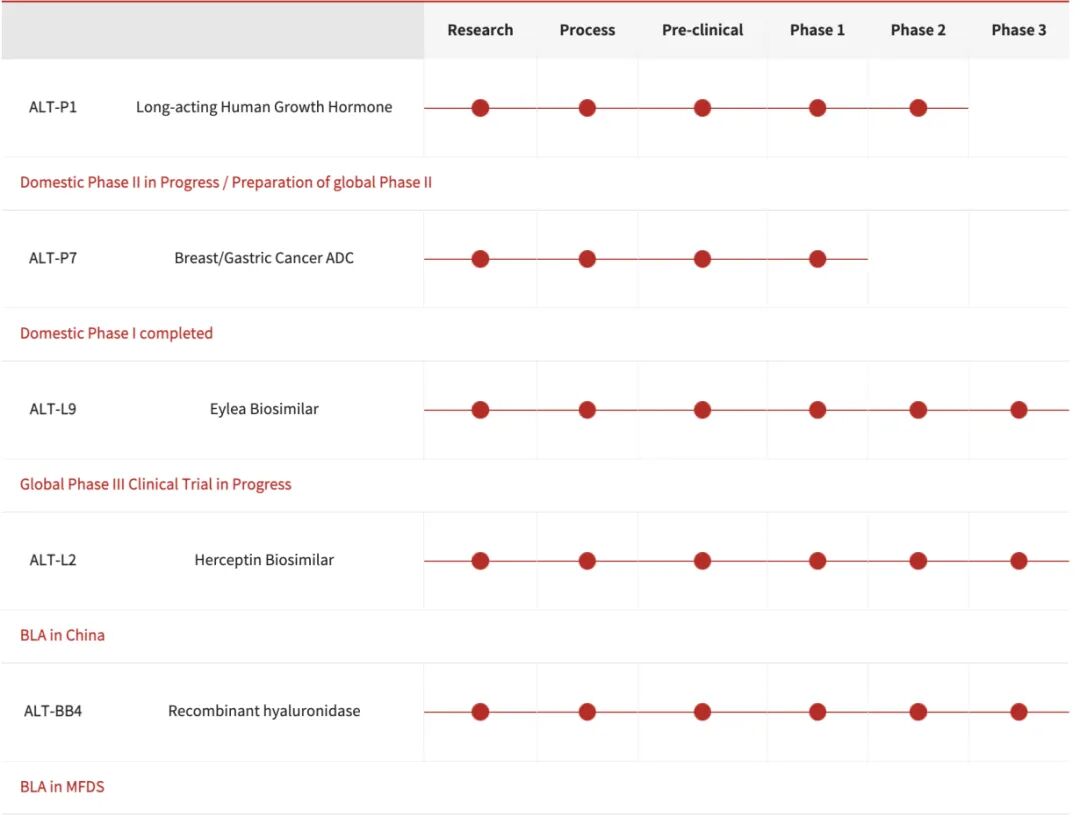
自成立以来Alteogen成功构建了三大技术平台:长效技术NexP™、ADC技术NexMab™,以及皮下注射(sc)技术Hybrozyme™。
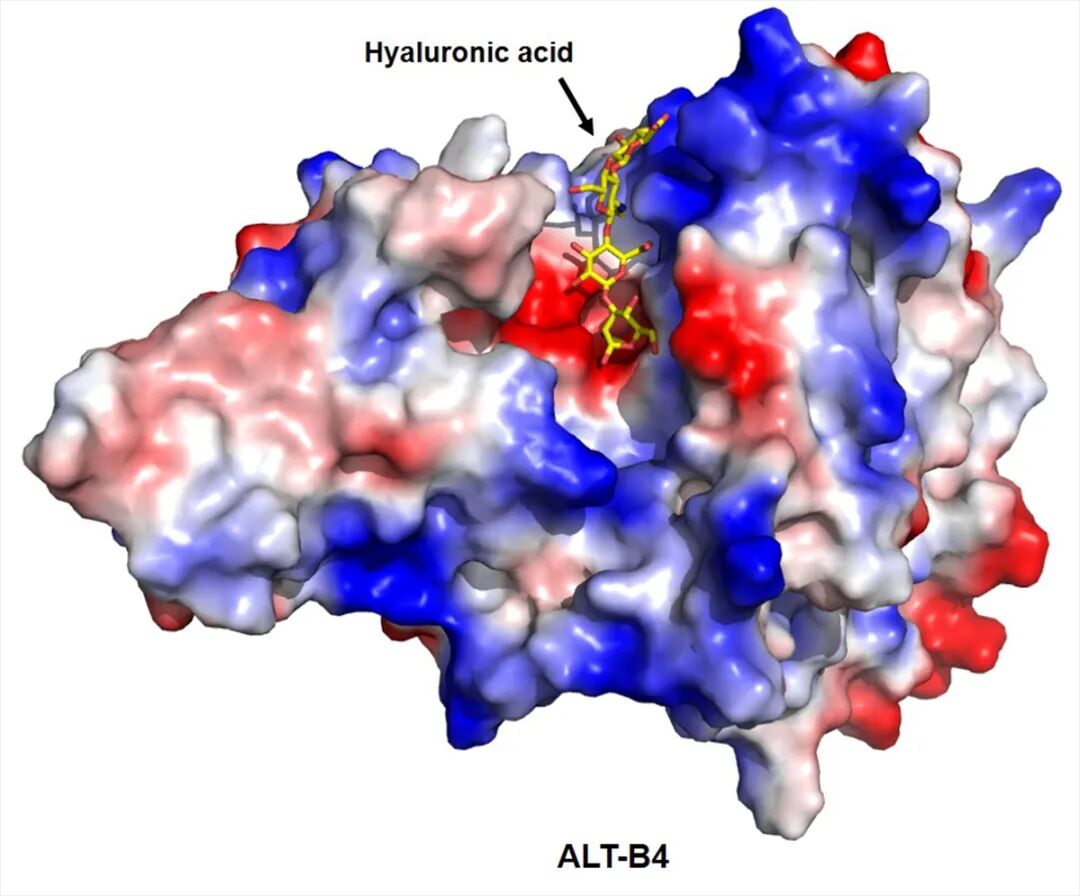
重Hybrozyme™技术由Alteogen自主研发,利用基于蛋白质工程的两种结构相似的酶的结构域交换,在保持固有催化机制的同时,提高了目标酶的构象灵活性和热稳定性。Alteogen通过该技术开发了专有的重组人透明质酸酶ALT-B4,能够将静脉注射(iv)药物改为皮下注射(sc)给药。酸酶
人透明质酸酶
目前全球范围内仅有Alteogen与美国的Halozyme Therapeutics等少数几家掌握了使用透明质酸酶将静脉制剂抗体药物转化为皮下注射制剂的技术,而Alteogen研发的新型重组人透明质酸酶在保持与Halozyme Therapeutic的重组人透明质酸酶(rHuPH20)相同的作用机理和酶活性的同时,增加了热稳定性,从而增加了蛋白质的稳定性,并提高了产量和经济性。(来自中国上海的宝济药业也在开发此类产品)
据报道,Alteogen已就该技术与包括默沙东、Intas、山德士在内的4家企业达成了合作,有两款产品正在开展临床试验。
基于Hybrozyme™技术,Alteogen还开发了重组人透明质酸酶产品(ALT-BB4,Tergase),除了作为抗体治疗药物或蛋白制剂的皮下注射剂型的佐剂之外,还将作为自有产品上市,用于皮肤科、眼科、整形外科和术后消肿止痛。2024年7月,Alteogen宣布韩国食品药品安全部(MFDS)批准了其Tergase®(重组透明质酸酶,研发代号ALT-BB4)的新药申请(NDA)。据报道,Tergase®的纯度超过99%,免疫原性较低。此次NDA申请得到了一项关键1期临床试验的支持,该试验达到主要终点,测试组皮内给药期间的药物过敏反应率显著低于美国FDA的建议,并且发现抗药抗体(ADA)的发生率为零。
【根据《通货膨胀削减法案》(IRA)实施的美国医疗保险药物价格谈判计划的修订指南,由透明质酸酶作为活性成分组成的固定剂量复方药物将被视为新药。这意味着透明质酸酶很可能成为制药商规避药品价格谈判的一种策略。
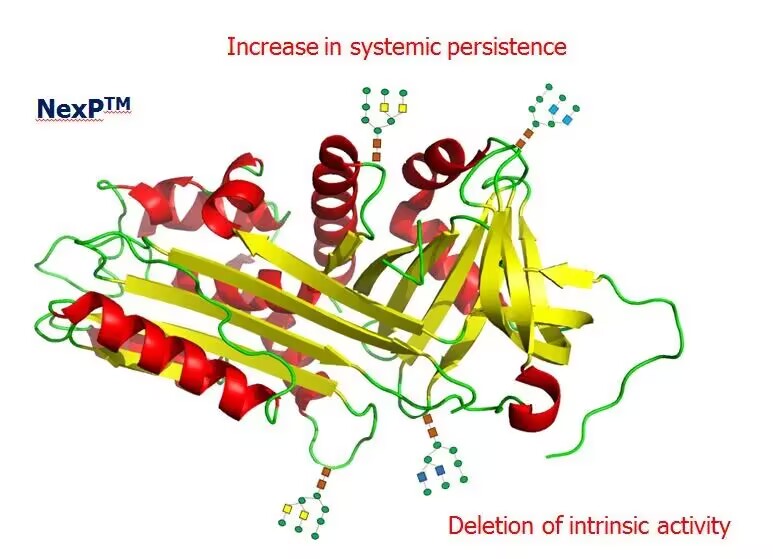
NexP™融合技术是Alteogen自主研发的第二代长效技术,使用人血中丰富的人A1AT(Alpha-1抗胰蛋白酶)蛋白作为蛋白质载体,可在蛋白质或肽的C端或N端融合,通过基因重组技术延长生物制剂的半衰期。通过NexP™技术开发的治疗性蛋白质或肽显示出优异的长效特性,而不会引起药物活性损失,在药代动力学和药效学临床前研究中显示,该技术显著增加了药物的体内半衰期并提高了效力,具有给药频率低、副作用少和临床疗效好等特点。NexP™技术是该公司开发下一代长效疗法的源头技术。
Alteogen正在使用其NexP™平台技术开发长效人生长激素ALT-P1。ALT-P1是Alteogen的旗舰biobetter产品,它结合了人生长激素和NexP™蛋白质载体。在临床前试验中,ALT-P1与第一代人类生长激素相比显示出更高的疗效和更长的半衰期。此外,ALT-P1的安全性已在围绕健康男性开展的1期临床试验中得到了明确证明。由于治疗剂量要求较低,预计ALT-P1比其他可用或正在开发的人生长激素显示出更低的毒性和/或更少的副作用。因此,有理由预期ALT-P1将被开发为同类治疗方案中的领先疗法。
目前,ALT-P1正在生长激素缺乏症患者中开展2期临床试验。
药融云数据www.pharnexcloud.com显示,Alteogen曾在2019年7月与巴西制药公司Cristalia达成一项合作协议,共同开发和商业化用于治疗生长障碍的ALT-P1。据Alteogen财报,双方于2021年底签署变更协议,最终临床试验结束后,Cristalia将获得南美地区的销售权,Alteogen将推动该产品在南美以外的全球范围内的许可审批。
财报,双方于2021年底签署变更协议,最终临床试验结束后,Cristalia将获得南美地区的销售权,Alteogen将推动该产品在南美以外的全球范围内的许可审批。
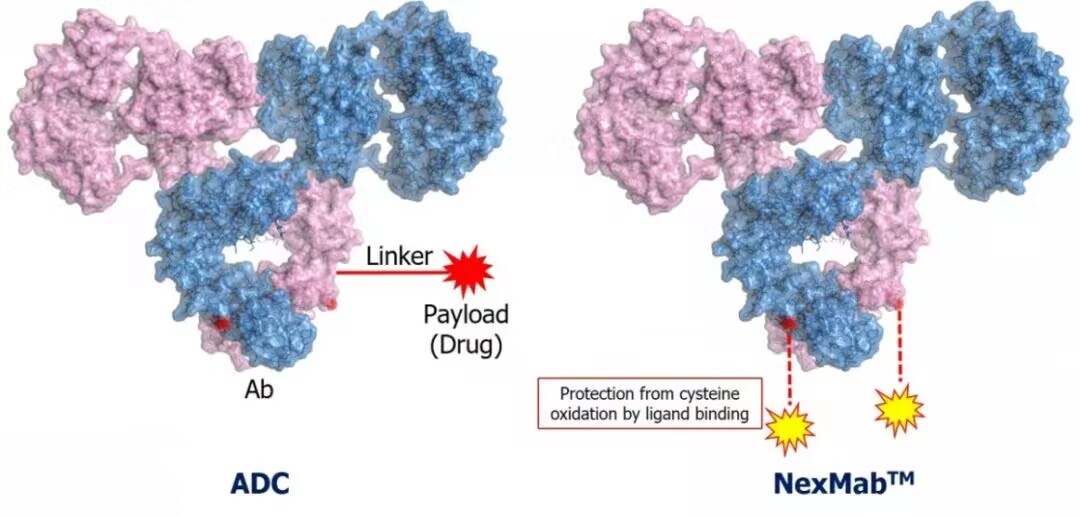
NexMab™ ADC技术是一种下一代ADC偶联技术,通过基因重组技术实现位点特异性偶联,通过选择性地将抗癌药物连接到抗体的特定区域(C-末端),使药物选择性地连接到抗体上,同时尽可能保留了抗体原来的结构,不影响抗体固有的活性,且在血液中不易降解,体内持久性良好,具有对癌细胞的高靶向性和强大的抗癌治疗效果。通过NexMab™技术开发的ADC药物能够兼具稳定性、疗效和经济可行性。
Alteogen正在使用NexMab™ ADC技术开发针对乳腺癌/胃癌的药物ALT-P7。ALT-P7是一种利用NexMab™ ADC技术开发的靶向HER2的ADC药物。据报道,HER2在20~25%的乳腺癌患者中过表达,在10~15%的胃癌患者中过表达。HER2一直是最成功的抗癌靶点之一。
ALT-P7的有效载荷药物与HER2靶向抗体进行了位点特异性偶联,与非位点特异性偶联相比,ALT-P7有望开发为更安全、更好的替代抗癌药物。目前ALT-P7已在韩国完成1期临床试验,据公司财报描述,该候选药物是首个在韩国完成1期临床试验的乳腺癌ADC药物,除了乳腺癌和胃癌之外,Alteogen正在考虑未来ALT-P7与其他药物联用治疗多种适应症。
Alteogen曾在2015年与三生制药达成达成独家许可协议,以在中国大陆、香港和澳门开发、制造和销售ALT-P7,该合作未见后续进展报道。
2017年11月,Alteogen与联宁生物(Levena Biopharma,是Sorrento Therapeutics的子公司)达成GMP合作协议,以支持其ADC产品ALT-P7开展临床研究。
Alteogen的生物类似药主要是与海外合作伙伴共同开发。基于研究人员在生物制剂方面拥有多年的研发和商业化经验,Alteogen一直在开发自己的高表达、高效工艺(上游和下游)的细胞系,以及优化的单克隆抗体生物类似药分析方法。Alteogen目前已利用自己的生产工艺(包括培养和纯化)迅速开发了两种高质量的生物类似药(Eylea的生物类似药ALT-L9以及Herceptin的生物类似药ALT-L2)。这些过程确保Alteogen的生物类似药与原始生物制剂的“可比性”。
Alteogen目前正在与战略联盟伙伴日本Kissei Pharmaceutical共同开发Eylea(阿柏西普)的生物类似药ALT-L9。Alteogen在2020年10月成立子公司Altos Biologics,负责开展ALT-L9的全球3期临床试验和海外销售。Altos Biologics于2021年3月与韩国国内主要眼科制药公司签署了国内的销售许可协议,并于2021年12月递交IND开始进行全球3期临床试验。2024年7月,Alteogen宣布子公司Altos Biologics已向欧洲药品管理局(EMA)递交了ALT-L9的上市许可申请(MAA),预计将在2025年之前获得批准,与原研阿柏西普的物质专利到期时间一致,并打算与全球潜在分销商协商许可协议。2024年9月,公司宣布已申请ALT-L9在韩国的上市许可。
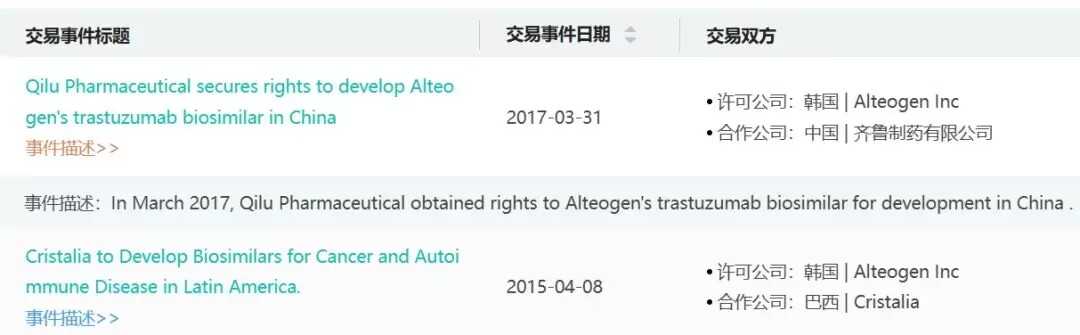
ALT-L2是Alteogen开发的Herceptin(曲妥珠单抗)的生物类似药,药融云数据www.pharnexcloud.com显示,Alteogen针对该药的开发合作伙伴是巴西制药公司Cristalia以及中国的齐鲁制药。2024年7月,齐鲁制药曲妥珠单抗生物类似药(安曲妥®,研发代号QL1701)的上市许可在国内获得批准,用于HER2阳性早期乳腺癌、转移性乳腺癌和转移性胃癌的治疗。此外,Alteogen正在考虑利用公司的Hybrozyme™技术开发Herceptin(曲妥珠单抗)皮下注射剂型的生物类似药,并与罗氏的曲妥珠单抗(皮下注射)完成了等效性测试。该公司正在考虑通过与全球制药公司进行技术转让以推出曲妥珠单抗皮下注射剂型的生物类似药。
2023全年,Alteogen公司总收入达到了965.2亿韩元(约合7400万美元),同比增长235.08%。其中有833.3亿韩元(6400万美元)来自于技术服务收入,主要涉及重组人透明质酸酶ALT-B4,占公司全年总收入的86.3%。全年销售成本为653.2亿韩元,毛利润为312.0亿韩元,销售一般管理费用为409.3亿韩元,营业亏损97.37亿韩元。全年研发费用合计976.0亿韩元(7500万美元),研发费用占销售收入比例为101.12%。